
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
I. Перегонка при обычном давлении
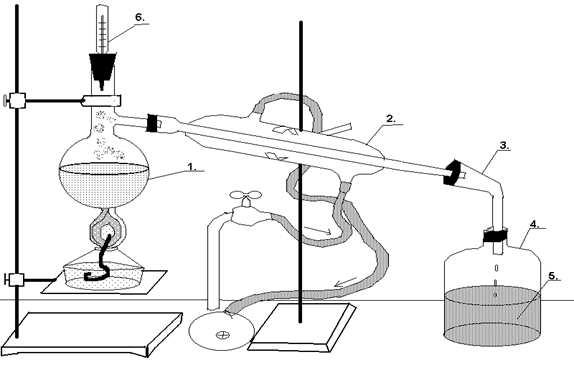
Для перегонки собирают прибор, состоящий из колбы Вюрца, прямого холодильника и приемника, как показано на рисунке 4.
|
Рис. 4 Прибор для перегонки жидкости.
1. Колба Вюрца , 2. Холодильник Либиха , 3. Аллонж,
4. Приемник, 5. Дистиллят , 6. Термометр.
При этом жидкость в колбе Вюрца не должна занимать более 2/3 ее объема. В колбу кладут бусинки, чтобы избежать внезапного вскипания
жидкости и попадания ее в холодильник. Термометр должен быть установлен так, чтобы его резервуар со ртутью находился посередине горла колбы, не касаясь ее, против или чуть ниже пароотводной трубки. Перед тем, как начать нагревание, проверяют надежность и правильность соединения всех частей прибора, осторожно заполняют холодильник водой и только после этого начинают нагревание.
Когда из смеси жидкостей с различными температурами кипения выделяют отдельные компоненты, то такая перегонка называется дробной (фракционной). Для этого колбу Вюрца заменяют круглодонной колбой с коротким горлом, в которое вставляют дефлегматор. В верхний открытый конец дефлегматора вставляют термометр, а пароотводную трубку соединяют с холодильником. Дефлегматор применяют для того, чтобы увеличить поверхность охлаждения паров испаряющей жидкости, что дает возможность перегонять жидкость в узких границах температур. Перегонка не должна проходить слишком быстро. Первая небольшая порция дистиллята - это примеси. Когда показания термометра соответствуют температуре кипения перегоняемого вещества, подставляют другой приемник, куда собирают перегоняемое вещество. Процесс заканчивают, когда в колбе остается небольшое количество жидкости, перегонять досуха нельзя.
Перегонка лежит в основе получения дистиллированной воды, которая широко используется во всех лабораториях для самых различных целей: приготовления растворов, различных реактивов, обработки посуды и т.д.
Дистиллированная вода – это вода очищенная от растворенных в ней минеральных солей, органических веществ и других примесей путем дистилляции (перегонки) водопроводной воды, то есть воду превращают в пар и конденсируют. Получают ее в перегонных аппаратах изготовленных из высококачественного стекла или стали. Обычно дистилляционная установка состоит из обогреваемой емкости (куба), имеющих разную величину и производительность, конденсатора и приемных емкостей. Дистиллированная вода всегда содержит незначительные примеси посторонних веществ, попадающих в нее из воздуха в виде пыли или вследствие выщелачивания стекла посуды, в которой храниться вода, или в виде следов металла трубки холодильника.
Для удаления следов металла используют обработку дистиллированной воды высоко активированным углем. Чтобы очистить воду от органических веществ, ее подвергают вторичной перегонке, добавляя в воду немного марганцево-кислого калия и несколько капель серной кислоты. Воду более высокой чистоты – бидистиллят, получают повторной перегонкой в специальных аппаратах – бидистилляторах, изготовленных обычно из кварцевого стекла.
Воду для лабораторных целей готовят обычно путем перегонки природной воды, очистки ее от СО2 и других примесей. Для ответственных физико-химических и аналитических исследований пользуются, как правило, дважды перегнанной водой («бидистиллатом»). Для перегонки лучше всего использовать аппаратуру из кварца.
Для разрушения органических примесей и связывания обычно присутствующих в воде ионов NH+4 и CL- рекомендуется добавить на каждый литр очищаемой воды 0,025 г KmnO4, затем через 0,5 ч раствор 0,5-1 г алюмокалиевых квасцов и еще через 1 ч раствор 0,66 г Na2HPO4. Воду выдерживают 0,5 ч и отфильтровывают осадок. Фильтрат кипятят 10 мин. И перегоняют с обычным холодильником, отбрасывая первую и последнюю фракции (10%) дистиллата.
Не рекомендуется всецело полагаться на перегонку как надежный способ получения дистиллированной воды удовлетворительного качества. Наиболее вероятными причинами загрязнения могут быть применение недостаточно чистой посуды в качестве приемника и часто имеющая место переброска воды в приемник при неравномерном кипении/
Поступающую в лабораторию дистиллированную воду следует испытывать на присутствие хлоридов и сульфатов. Необходимо всегда проводить контроль рН воды: при добавлении к 10 мл испытуемой воды одной капли фенолового красного окраска должна быть желтой или желто- розовой; при добавлении одной капли метилового красного окраска должна быть чисто желтой.
Простой и эффективный метод контроля чистоты дистиллированной воды, позволяющий установить факт переброски воды в приемник, предложен Д.Н. Финкельштейном. Метод основан на исключительно высокой чувствительности к ионам двухвалентных металлов индикатора эриохром черный Т.
При добавлении 1 капли индикаторного раствора к 100 мл испытуемой воды и взбалтывании должна получиться сине-голубая окраска; примесь хотя бы одной капли водопроводной воды вызовет появление буроватой или малиновой окраски.
Индикаторный раствор готовят, растворяя 1 г солянокислого гидроксиламина и 0,25 г индикатора эриохром черный Т в 20 мл NH4OH (пл. 0,91) и разбавляя после полного растворения этиловым спиртом до 50 мл.
Если совместить этот метод проверки с одновременным контролем рН, то можно надежно обеспечить должную чистоту дистиллированной воды.
1. Для очень ответственных работ ( например, определение атомных весов элементов) воду очищают перегоняя ее дважды с щелочным раствором KmnO4 в стеклянной аппаратуре на шлифах. Затем дистиллят перегоняют третий раз из колбы стекла “пирекс” ( еще лучше из кварцевой колбы) с оловянным холодильником, при все части прибора соединяют на шлифах или в стык. Чистую воду собирают в колбу из иенского стекла, кварца или полиэтилена.
2. Есть указания, что очень чистая вода, пригодная для измерений электропроводности, получается дробным вымораживанием дистиллированной воды. Первые порции льда наиболее чисты.
3. Для получения дистиллированной воды, на содержащей CO2 ( по ГОСТ 4517-65), воду кипятят 0,5 ч до выделения крупных пузырей. Затем воду охлаждают, при этом колбу закрывают пробкой с трубкой, которую соединяют со склянкой Тищенко, содержащей 20%-ный раствор NaOH или КОН.
4. Для получения дистиллированной воды без кислорода ( по ГОСТ 4517-65) воду кипятят 2 ч, после чего охлаждают, закрыв колбу пробкой с газоотводной трубкой, которую соединяют со склянкой Тищенко, заполненной раствором пирогаллола. Раствор пирогаллола готовят растворением 8 г пирогаллола в 100 мл воды ( раствор А) и 120 г КОН в 80 мл воды ( раствор Б). Перед применением растворы А и Б смешивают в отношении 1:6. Смешение проводят непосредственно в той склянке Тищенко, которая предназначена для поглотителя кислорода.
5. Значительно более совершенный способ очистки, пригодный для получения воды высокой чистоты, основан на использовании ионообменных смол. Применение смешанных смол (катионит + анионит) позволяет добиться удаления практически всех катионов и анионов и приготовить воду с удельным сопротивлением 20-24 МОм*см. можно, например, пропускать дистиллированную ( или водопроводную ) воду через колонку, содержащую смесь отечественных ионообменных смол КУ-2 и АВ-17, отсеянных от пылевидных частиц (0,4 мм ). Катионит КУ-2 предварительно многократно промывают 3-4 %-ным раствором NaOH или КОН со скоростью 10 мл/ мин для удаления органических примесей, затем 5 %-ной HCL (х.ч.) для извлечения железа и, наконец, водой до нейтральной реакции фильтрата. Для очистки значительных количеств дистиллированной воды (100 л/ч) ее пропускают через фильтр с активным углем БАУ, через две колонки с анионитом АВ-17, через две колонки с катионитом КУ-2 и через шесть колонок со смесью ионитов АВ-17 и КУ-2. Все колонки и коммуникации должны быть изготовлены из винипласта, полиэтилена или фторопласта-4*. Содержание примесей AL, B, Fe, Ca, Cu, Mn, Mg, As, Pb, P, Se в очищенной с помощью ионообменных смол воде составляет 10-7—10-8%, содержание F. Si. CL менее 5*10-6%. Особо чистую воду необходимо хранить в сосудах из фторопласта-4 или полиэтилена, но следует иметь в виду, что длительное хранение приводит к загрязнению воды.
6. Дистиллированную воду удовлетворительного качества можно получить перегонкой в так называемых аптечных электрических дистилляторах, хотя иногда наблюдается переброс воды в приемник.
II Перегонка при уменьшенном давлении (вакуум-перегонка).
Ее применяют, если в обычных условиях жидкость не выдерживает нагревания до нужной температуры. Установка для перегонки под вакуумом более сложна и состоит из колбы Клайзена (рис.5) или колбы Арбузова (рис.6), прямого холодильника, приемников, манометра, предохранительной склянки и водоструйного вакуум-насоса.

|

|
Рис .5 Колба Клайзена
Рис.6 Колба Арбузова
Прямое колено горла колбы вставляют на пробке капилляр, доходящий почти до дна колбы. В изогнутое колено сверху вставляют термометр. Пароотводную трубку при помощи пробки соединяют с холодильником, который в свою очередь соединен с приемником. Приемник соединяют с водоструйным или другим вакуум-насосом через предохранительную склянку с помощью трехходового крана. В систему также включен ртутный манометр для измерения остаточного давления в приборе. Самым важным при сборке прибора является плотность всех мест соединения. Пробки должны быть подобраны так, чтобы нигде не происходило просачивание воздуха, на них наносится густой слой вакуумной замазки, вазелина или нитроцеллюлозы. Если вакуум-насос работает нормально, то вскоре после его включения манометр должен показывать довольно низкое давление. Если этого не происходит, то надо вновь тщательно проверить се места соединения.
При помощи трехходового крана всю систему можно быстро отключить от вакуум-насоса, а также впустить воздух в прибор после окончания перегонки. Капилляр, вставляемый в прямое горло колб, нужен для регулирования кипения жидкости. Через него в перегонную колбу поступают пузырьки воздуха. Это должно происходить со скоростью 1 - 2 пузырька в сек, большая скорость может затруднить достижение требуемого разряжения. Для всех соединений используют только толстостенные резиновые трубки. Колбу с жидкостью нагревают медленно, на 1 - 2 С в минуту.
После проведения вакуумной перегонки прежде всего прекращают нагревание, затем трехходовым краном отсоединяют прибор от вакуум-насоса. Прибору дают остыть, затем краном осторожно и медленно впускают воздух. Когда давление в приборе уравняется с наружным, отсоединяют приемник, вынимают термометр из колбы, затем снимают колбу. Еще до этого прекращают подачу воды в холодильник.
III. Перегонка с водяным паром. Ее применяют для отгонки веществ, нерастворимых в воде. Для этого собирают прибор, состоящий из парообразователя (паровика), водоотделителя, холодильника и приемника.
Жидкость, подлежащую перегонке, наливают в перегонную колбу и нагревают почти до кипения, продолжая делать это в течении всего процесса. Это делают для того, чтобы избежать конденсации пара в колбе и увеличить объем жидкости в ней. Получаемый с помощью паровика водяной пар пропускают через жидкость в перегонной колбе, при этом отгоняемое вещество уносится паром в холодильник, в котором образуется вода и отгоняемое вещество. Конденсат стекает в приемник, подставляемый под нижний конец холодильника. Воду и перегоняемое вещество, (если оно жидкость) отделяют при помощи делительной воронки. Если перегнанное вещество кристаллическое, то после быстрого охлаждения жидкую часть сливают, а кристаллы высушивают.
После окончания перегонки сначала отсоединяют паровичок, после чего прекращают нагревание. Окончательную разборку прибора проводят только после охлаждения. Надо быть осторожным при работе с паровичком, чтобы не получить ожог паром. Основным отличаем прямой и обратной перегонки является холодильный узел. Если стоит прямой холодильник и конденсируемая жидкость попадает в другой сосуд – то это прямая перегонка, если стоит обратный холодильник и конденсируемая жидкость после охлаждения попадает обратно в нагревательный сосуд – то это обратная перегонка (так, например, получают реактив Фолина для определения белка по Лоури).
Выпаривание, упаривание и перекристаллизация.
Выпариванием называется процесс, в при котором из раствора удаляют весь растворитель, в результате чего будет выделено растворенное вещество. Если же из раствора удаляют только часть растворителя, повышая тем самым концентрацию растворенного вещества, то это будет упаривание. Эти операции проводят в фарфоровых, стеклянных, кварцевых или эмалированных выпаривательных чашках.
При проведении выпаривания в водяной бане чашка должна быть помещена в баню не менее чем на 3/4 своей высоты. Жидкость, которая подвергается процедуре, должна занимать не более 2/3 в чашке по высоте. При этом уровень жидкости в чашке должен быть ниже уровня колец бани, т.к. при недостаточном нагревании верхней части кристаллы будут “всползать” по стенкам вверх. Периодически надо перемешивать выпариваемую жидкость, разбивая корочку кристаллов на поверхности.
Работу с водяными растворами можно проводить прямо на электроплите, работать с органическими растворителями можно только под тягой.
Перед проведением упаривания проводят предварительный расчет , до какого объема следует упарить жидкость, чтобы получить нужную концентрацию. Окончание упаривания можно определить путем определения плотности раствора.
Перекристализация. Ее проводят с целью очистки и для разделения кристаллических веществ. Процесс основан на свойстве кристаллических веществ изменять свою растворимость в данном растворителе в зависимости от температуры. Как правило, с повышением температуры растворимость веществ повышается и наоборот, причем для разных веществ температура образования насыщенных растворов различна.
Перекристаллизацию обычно применяют для очистки разных растворимых солей. Этим методом можно получить хорошо очищенное твердое вещество, но при этом велики потери реактива. Перекристаллизацию можно проводить не только из водных, ни и из спиртовых, бензольных растворов.
Вещество, которое нужно перекристаллизовать, растворяют в воде или органическом растворителе до получения насыщенного раствора.
Затем горячий раствор отфильтровывают под давлением с помощью воронки для горячего фильтрования. Под воронку ставят кристаллизатор, погруженный в снег, лед, холодильную смесь или холодную воду. При охлаждении из отфильтрованного насыщенного раствора выпадают мелкие кристаллы. Величина их зависит от скорости охлаждения. При быстром охлаждении образуются мелкие формы. Чем кристаллы меньше, тем чище получаемое вещество. При медленном охлаждении образуются крупные, менее чистые кристаллы, внутри которых даже может оставаться раствор, поэтому очень важно провести быстрое охлаждение. Кристаллы отделяют, слив маточную жидкость, или путем фильтрации на воронке Бюхнера, затем их высушивают. Маточные растворы, оставшиеся после процедуры, можно упарить и провести повторную перекристаллизации, но полученное вещество будет уже менее чистым. Способом перекристаллизации можно получать очень хорошо очищенные вещества, проведя процедуру несколько раз, но при этом велики потери реактива.
Возгонка (сублимация)
Некоторые твердые вещества при нагревании переходят сразу из твердого состояния в газообразное, минуя жидкое и обратно. В подобных случаях говорят, что вещество не перегоняется, а возгоняется (сублимируется). Возгонкой можно очищать йод, серу, нафталин, хлористый аммоний, хиноны.
Простейшим прибором для возгонки является химический стакан без носика, закрытый часовым стеклом выпуклой стороной внутрь стакана. В стакан помещают небольшое количество вещества, которое надо очистить , в углубление стекла наливают холодную воду, кладут снег или лед. При осторожном нагревании происходит возгонка твердого вещества, пары которого, охлаждаясь у поверхности стекла, собираются на нем в виде кристаллов, которые потом счищают стеклянной палочкой. Они называются возгонном. Для получения особо чистых веществ возгон подвергают повторной процедуре.
Преимущества возгонки по сравнению с перекристаллизацией в том, что в результате ее , как правило, сразу же получается чистый продукт и возгонку можно проводить даже с небольшим количеством вещества.
ВЫСУШИВАНИЕ - Это отделение воды или ее паров, жидких органических растворителей или их паров, которые могут содержаться в газах, жидкостях и твердых телах.
Высушивание твердых веществ.
Обычно осадки, которые получают при фильтровании, содержат некоторое количество растворителя, Удалить его можно сушкой. Выбор метода высушивания зависит от физических и химических свойств веществ.
Твердые вещества можно сушить на открытом воздухе или при нагревании. На воздухе при комнатной температуре можно сушить негигроскопические вещества. Их обычно рассыпают тонким слоем на листе фильтровальной бумаги, прикрывая сверху другим. Для ускорения процесса можно сверху, параллельно веществу продувать воздух. Высушенное вещество пересыпают в заранее приготовленную емкость и плотно закрывают. Также высушивание можно проводить в сушильных шкафах, на различных банях с выпаривательных чашках. Нельзя нагревать сосуд голым пламенем, так как это может вызвать местные перегревы и привести к распаду вещества.
Широко применяется высушивание в эксикаторе, особенно если вещество нельзя нагревать. Для высушивания паров воды или спирта в эксикатор помещают едкий натр, хлорид кальция, фосфорный ангидрид. Если надо избавиться от паров диэтилового эфира, используют парафин.
Высушивание газов от содержащихся в них паров воды или органических растворителей проводят путем пропускания их через жидкие или твердые поглотители (адсорбенты). Для сушки газов удобно использовать серную кислоту, если она не вступает с ними в реакцию. С ее помощью осушают кислород и водород, азот, углекислый газ, хлор, сернистый газ. Из твердых осушителей применяют окись фосфора - для кислых и нейтральных газов, и натронная известь – для основных и нейтральных газов. Также используют окись алюминия, силикагель и подобные им вещества, хлоркальциевые трубки. Самым важным является инертность поглотителей к очищенному газу. При использовании жидких поглотителей часто применяют предохранительные склянки, склянки Вульфа (рис.7), Дрекселя или Тищенко. Поглотитель не должен занимать более 1/4 высоты склянки. Для лучшего освобождения газов применяют несколько поглотителей, соединенных последовательно.

|

|
Рис.7.
Склянка Вульфа
Рис. 8. Газовая колонка
Твердые осушающие вещества помещают в склянки или колонку (рис.8), через которую продувают газ, который нужно очистить. Чтобы осушитель в колонке не слеживался, его смешивают с асбестовым волокном, пемзой, стекловатой.
Высушивание органических жидкостей.
Для этого применяют только твердые водоотнимающие или водопоглащающие вещества. Вода, содержащаяся в органическом растворителе, может образовывать кристаллогидраты с высушивающим веществом, или вступать с ним в химическую реакцию или просто поглощаться. Хорошим высушивающим средством для многих органических жидкостей является ангидрион Mg(ClO4)2, так же применяют активированную окись алюминия и ряд других. Для высушивания жидкости в сосуд в котором она находиться, осторожно вносят соответствующее высушивающее вещество, сосуд осторожно встряхивают и плотно закрывают. Процесс высушивания длиться от нескольких часов, до нескольких суток. Затем жидкость перегоняют. Чтобы не произошло поглощение влаги из воздуха, приемник плотно закрывают пробкой с аллонжем или хлоркальциевой трубкой.
Вопросы для проверки исходного уровня знаний
1. Общая характеристика материалов используемых для изготовления лабораторной химической посуды. Основные требования к химической посуде. Классификация химической посуды.
2. Примеры посуды общего назначения и правила работы с ней.
3. Примеры посуды специального назначения и правила работы с ней.
4. Виды мерной посуды правила работы с цилиндром и мензуркой.
5. Правила работы с мерной колбой, бюреткой.
6. Правила работы с пипеткой.
7. Механическая очистка химической посуды.
8. Химическая очистка лабораторной посуды.
9. Проверка мерной посуды.
10. Фильтрование как метод очистки веществ. Фильтрующие материалы.
11. Способы фильтрования
12. Перегонка при обычном давлении.
13. Оценка чистоты дистиллированной воды.
14. Перегонка при уменьшенном давлении.
15. Перегонка с водяным паром. Отличие прямой и обратной перегонки.
16. Выпаривание, упаривание и перекристализация как методы очистки веществ.
17. Возгонка (сублимация) и высушивание как метод очистки веществ.
Дата добавления: 2015-01-01; просмотров: 1642; Мы поможем в написании вашей работы!; Нарушение авторских прав |