
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Основы термодинамики
Краткая теория
 Средняя кинетическая энергия поступательного движения одной молекулы идеального одноатомного газа
Средняя кинетическая энергия поступательного движения одной молекулы идеального одноатомного газа
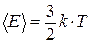 ,
,
где k – постоянная Больцмана, T – абсолютная температура.
 Внутренняя энергия идеального газа равна:
Внутренняя энергия идеального газа равна:
 , или
, или
 , или
, или
 ,
,
где i – число степеней свободы молекул, равное 3 для одноатомного газа; 5 для двухатомного и 6 для многоатомного с нелинейными молекулами; R – универсальная газовая постоянная, T – абсолютная температура, 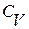 – молярная теплоёмкость газа при постоянном объёме;
– молярная теплоёмкость газа при постоянном объёме;  – количество вещества ( число молей), m – масса газа, μ – его молярная масса, p – давление газа, V – его объём.
– количество вещества ( число молей), m – масса газа, μ – его молярная масса, p – давление газа, V – его объём.
 Уравнение состояния идеального газа (уравнениеМенделеева-Клапейрона:
Уравнение состояния идеального газа (уравнениеМенделеева-Клапейрона:
 , или
, или 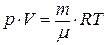 ,
,
где m – масса газа; µ – его молярная масса; Т – термодинамическая температура; 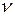 – количество вещества; R – универсальная газовая постоянная.
– количество вещества; R – универсальная газовая постоянная.
 Уравнение изотермического процесса (
Уравнение изотермического процесса (  ):
):
 , или
, или  .
.
 Уравнение изохорического процесса (
Уравнение изохорического процесса (  ):
):
 , или
, или  .
.
 Уравнение изобарического процесса (
Уравнение изобарического процесса ( 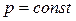 ):
):
 , или
, или  .
.
 Элементарная работа газа при увеличении объёма на
Элементарная работа газа при увеличении объёма на  равна:
равна:
 ,
,
где р – давление газа.
 Работа газа при изменении объёма от V1 до V2:
Работа газа при изменении объёма от V1 до V2:
 .
.
При изобарном процессе работа равна  .
.
 Теплоемкость тела – это количество теплоты, необходимое для нагревания этого тела на один градус (кельвин):
Теплоемкость тела – это количество теплоты, необходимое для нагревания этого тела на один градус (кельвин):
 .
.
 Удельная теплоемкость – это количество теплоты, необходимое для нагревания единицы массы вещества на один градус:
Удельная теплоемкость – это количество теплоты, необходимое для нагревания единицы массы вещества на один градус:
 .
.
 Удельная теплоемкость – это количество теплоты, необходимое для нагревания одного моля вещества на один градус:
Удельная теплоемкость – это количество теплоты, необходимое для нагревания одного моля вещества на один градус:
 .
.
 Связь между молярной (С) и удельной (с) теплоемкостями:
Связь между молярной (С) и удельной (с) теплоемкостями:
 ,
,
где μ – молярная масса.
 Молярная теплоёмкость идеального газа при постоянном объёме:
Молярная теплоёмкость идеального газа при постоянном объёме:
 ,
,
где i – число степеней свободы молекул; R – универсальная газовая постоянная. Для одноатомных газов  .
.
 Молярная теплоёмкость идеального газа при постоянном давлении:
Молярная теплоёмкость идеального газа при постоянном давлении:
 ,
,
где i – число степеней свободы молекул; R – универсальная газовая постоянная. Для одноатомных газов  .
.
 Уравнение Майера:
Уравнение Майера:
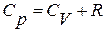 .
.
 Количество теплоты, поглощённой в процессах:
Количество теплоты, поглощённой в процессах:
– нагревания  ,
,
– плавления:  ,
,
– парообразования  ,
,
где  – удельная теплоемкость тела,
– удельная теплоемкость тела,  – удельная теплота плавления, r – удельная теплота парообразования, m – масса.
– удельная теплота плавления, r – удельная теплота парообразования, m – масса.
 Количество теплоты, выделившейся в процессе сгорания топлива:
Количество теплоты, выделившейся в процессе сгорания топлива:
 ,
,
где  – удельная теплота сгорания топлива, m – его масса.
– удельная теплота сгорания топлива, m – его масса.
 Первый закон (первое начало) термодинамики: количество теплоты Q, сообщенное системе, идет на увеличение её внутренней энергии
Первый закон (первое начало) термодинамики: количество теплоты Q, сообщенное системе, идет на увеличение её внутренней энергии  и совершение этой системой работы
и совершение этой системой работы  против внешних сил:
против внешних сил:
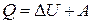 .
.
Первое начало термодинамики:
– для изохорного процесса  ;
;
– для изобарного процесса:  ;
;
– для изотермического процесса:  ;
;
– для адиабатного процесса:  .
.
 Коэффициент полезного действия (КПД) тепловой машины:
Коэффициент полезного действия (КПД) тепловой машины:
 ,
,
где  – полезная работа, совершаемая машиной;
– полезная работа, совершаемая машиной; 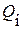 – количество теплоты, полученное рабочим телом от нагревателя;
– количество теплоты, полученное рабочим телом от нагревателя;  – количество теплоты, отданное рабочим телом холодильнику. Идеальная тепловая машина, работающая по циклу Карно (рис.5.1), при заданных температурах нагревателя
– количество теплоты, отданное рабочим телом холодильнику. Идеальная тепловая машина, работающая по циклу Карно (рис.5.1), при заданных температурах нагревателя  и охладителя
и охладителя  , имеет максимальный КПД, не зависящий от природы рабочего тела:
, имеет максимальный КПД, не зависящий от природы рабочего тела:
 .
.
 |
Дата добавления: 2014-10-31; просмотров: 326; Мы поможем в написании вашей работы!; Нарушение авторских прав |