
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Работа и количество тепла. Первый закон термодинамики. Работа при равновесном и неравновесном изменении объема системы.
Пусть внутренняя энергия системы изменилась за счет взаимодействия с внешней средой на величину dU. По закону сохранения и превращения энергии таким же по абсолютной величине должно быть изменение энергии тех тел окружающей среды, с которыми провзаимодействовала система.
Полная работа, которой обменивается рассматриваемая система с окружающими телами,
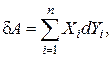 (2.3.8)
(2.3.8)
где n – число разнородных воздействий (механических, электрических, магнитных и т. д.) на тело. Элементарную работу, совершаемую системой над внешними телами, условились считать положительной  ; если работа совершается над системой, то ей приписывается отрицательный знак
; если работа совершается над системой, то ей приписывается отрицательный знак 
Работа – это способ обмена энергией между системой и окружающей средой. Если такового обмена нет, то ни у рассматриваемой системы, ни у окружающей среды нет определенного количества работы, т. е. работа не является функцией состояния.
Способ изменения внутренней энергии системы не сопровождается макроскопической (видимой) работой, т. е. при этом способе внешние тела не перемещаются или не изменяются действующие на систему внешние поля. Этот способ изменения внутренней энергии системы называют теплообменом (теплопередачей) и заключается он в том, что рассматриваемая система приводится в тепловой контакт с внешней средой, имеющей температуру, отличную от температуры самой системы.
Количество энергии, которым обменивается система и окружающая среда в процессе теплообмена, называют количеством теплоты.
Количество теплоты проявляется только в процессе обмена энергией системы и окружающей среды. У тела может быть только определенное количество внутренней энергии. Поэтому внутренняя энергия – функция состояния, а теплота, как и работа, не является функцией состояния.
Все три введенные величины – внутренняя энергия, работа и теплота входят в уравнение первого закона термодинамики. Согласно этому закону, количество теплоты 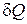 , полученное системой, расходуется наизменение внутренней энергии
, полученное системой, расходуется наизменение внутренней энергии  и на совершение системой работы
и на совершение системой работы 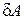 :
:
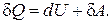 (2.3.9)
(2.3.9)
Если система частиц изолирована, т. е. не обменивается энергией с окружающей средой ни в форме работы 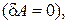 ни в форме теплоты
ни в форме теплоты 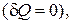 то
то 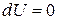 и внутренняя энергия сохраняется (U = const). Таким образом, первый закон термодинамики – это приложение более общего закона сохранения энергии к термодинамическимпроцессам, при которых происходит превращение работы, понимаемой в обобщенном смысле (2.3.8), в теплоту и теплоты в работу.
и внутренняя энергия сохраняется (U = const). Таким образом, первый закон термодинамики – это приложение более общего закона сохранения энергии к термодинамическимпроцессам, при которых происходит превращение работы, понимаемой в обобщенном смысле (2.3.8), в теплоту и теплоты в работу.
Пусть газ, заключенный в цилиндр и закрытый сверху невесомым подвижным поршнем, находится в равновесии. Это значит, что давление газа p равно внешнему давлению 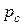 среды (рис. 24).
среды (рис. 24).
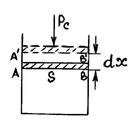
Р и с.24
Положим, что газ бесконечно медленно (равновесно) расширился за счет полученного тепла и поршень переместился на 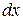 из положения АВ в положение
из положения АВ в положение 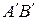 . Вычислим работу, которую при этом совершил газ. Работа эта заключается в том, что газ при расширении преодолевает внешнее давление
. Вычислим работу, которую при этом совершил газ. Работа эта заключается в том, что газ при расширении преодолевает внешнее давление 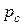 , под которым он находится. По определению работы
, под которым он находится. По определению работы
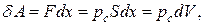 (2.4.1)
(2.4.1)
где 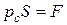 – внешняя сила давления, преодолеваемая газом, а
– внешняя сила давления, преодолеваемая газом, а 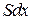 – увеличение объема газа при его расширении,
– увеличение объема газа при его расширении, 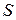 – площадь поршня.
– площадь поршня.
Работа расширения, совершаемая газом, при конечном изменении объема
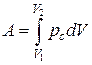 (2.4.2)
(2.4.2)
Ясно, что работа расширения против сил внешнего давления производится только тогда, когда изменяется объем тела 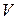 и когда внешнее давление
и когда внешнее давление 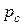 не равно нулю. Если же
не равно нулю. Если же 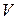 сохраняется постоянным, то какие бы изменения ни претерпевали любые другие параметры, характеризующие состояние газа (температура, давление, внутренняя. энергия и т. д.), работа расширения всегда будет равна нулю. С другой стороны, если объем газа изменяется, но внешнее давление все время равно нулю
сохраняется постоянным, то какие бы изменения ни претерпевали любые другие параметры, характеризующие состояние газа (температура, давление, внутренняя. энергия и т. д.), работа расширения всегда будет равна нулю. С другой стороны, если объем газа изменяется, но внешнее давление все время равно нулю 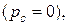 как это имеет место при расширении газа в вакуум, то работа расширения тоже равна нулю. Поэтому с точки зрения возможности совершения газом работы против внешнего давления
как это имеет место при расширении газа в вакуум, то работа расширения тоже равна нулю. Поэтому с точки зрения возможности совершения газом работы против внешнего давления 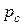 параметр
параметр 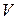 является жестко связанным с этим давлением, как говорят, сопряжен с ним.
является жестко связанным с этим давлением, как говорят, сопряжен с ним.
Знак работы определяется знаком 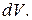 Так как абсолютное давление – существенно положительная величина, то при расширении
Так как абсолютное давление – существенно положительная величина, то при расширении 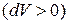 работа производится газом над внешней средой и, как видно из соотношений (3.4.1–3.4.2), положительна, при сжатии
работа производится газом над внешней средой и, как видно из соотношений (3.4.1–3.4.2), положительна, при сжатии  работа совершается внешней средой над газом и, как видно из тех же соотношений, отрицательна.
работа совершается внешней средой над газом и, как видно из тех же соотношений, отрицательна.
Формулы (2.4.1–2.4.2) справедливы не только для газов, но и для жидких и твердых тел. Рассмотрим, например, твердое тело, помещенное в жидкую или газообразную среду, которая при отсутствии внешних полей оказывает одинаковое давление на любые участки поверхности этого тела (рис. 25)

Р и с. 25
Постоянство давления 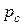 легко объясняется тем, что молекулы среды, находящейся в состоянии равновесия, движутся по всем направлениям с одинаковой вероятностью, с одинаковыми средними скоростями и на каждую единицу поверхности тела приходится в среднем одинаковое число ударов молекул одинаковой силы (закон Паскаля). При наличии внешнего поля силы тяжести давление
легко объясняется тем, что молекулы среды, находящейся в состоянии равновесия, движутся по всем направлениям с одинаковой вероятностью, с одинаковыми средними скоростями и на каждую единицу поверхности тела приходится в среднем одинаковое число ударов молекул одинаковой силы (закон Паскаля). При наличии внешнего поля силы тяжести давление 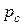 также можно считать постоянным на всей поверхности тела, если размеры его таковы, что можно пренебречь изменениями гидростатического давления.
также можно считать постоянным на всей поверхности тела, если размеры его таковы, что можно пренебречь изменениями гидростатического давления.
Пусть при расширении тела элементарные участки его поверхности 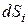 переместились по нормали к ним на расстояние
переместились по нормали к ним на расстояние 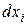 . Тогда работа на i-м участке
. Тогда работа на i-м участке
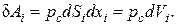
Полная работа тела по увеличению объема на 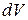
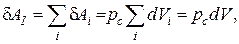
что совпадает с формулой (2.4.1).
Чтобы процесс был равновесным, он должен протекать бесконечно медленно. При этом давление газа 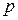 и внешнее давление среды
и внешнее давление среды 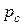 отличаются на бесконечно малую величину, т. е. для равновесных процессов справедливо равенство
отличаются на бесконечно малую величину, т. е. для равновесных процессов справедливо равенство
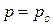 (2.4.3)
(2.4.3)
Поэтому формулы (2.4.1–2.4.2) для равновесного процесса приобретают вид:
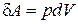 , (2.4.4)
, (2.4.4)
 (2.4.5)
(2.4.5)
где 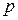 – давление газа (внутреннее давление в системе), которое может быть вычислено из уравнения состояния, например, из уравнения Менделеева – Клапейрона, если газ идеальный. Особо отметим, что формулы (2.4.4–2.4.5) справедливы только для равновесных процессов. Если процесс неравновесный, то давление газа отличается от давления окружающей среды на конечную величину. В этом случае расширение газа протекает с конечной скоростью, внешнее давление
– давление газа (внутреннее давление в системе), которое может быть вычислено из уравнения состояния, например, из уравнения Менделеева – Клапейрона, если газ идеальный. Особо отметим, что формулы (2.4.4–2.4.5) справедливы только для равновесных процессов. Если процесс неравновесный, то давление газа отличается от давления окружающей среды на конечную величину. В этом случае расширение газа протекает с конечной скоростью, внешнее давление 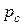 меньше давления
меньше давления 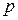 газа на конечную величину и, соответственно, полезная работа
газа на конечную величину и, соответственно, полезная работа  при неравновесном процессе меньше полезной работы
при неравновесном процессе меньше полезной работы 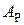 при равновесном процессе, т. е.
при равновесном процессе, т. е.
 . (2.4.6)
. (2.4.6)
При неравновесном сжатии, наоборот, внешнее давление больше давления газа, поэтому и затраченная работа на сжатие больше, чем в случае равновесного процесса, т. е.
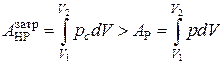 (2.4.7)
(2.4.7)
При неравновесных процессах работа расширениявсегда меньше а работа сжатия больше, чем при равновесных процессах.
Дата добавления: 2015-04-18; просмотров: 823; Мы поможем в написании вашей работы!; Нарушение авторских прав |