
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Фагоцитирующие клетки организма.
Защитная роль подвижных клеток крови и тканей была впервые обнаружена И. И. Мечниковым в 1883 г. Он назвал эти клетки фагоцитами и сформулировал основные положения фагоцитарной теории иммунитета.Фагоцитоз - поглощение фагоцитом крупных макромолекулярных комплексов или корпускул, бактерий. Клетки-фагоциты: нейтрофилы и моноциты/макрофаги. Фагоцитировать могут также эозинофилы (наиболее эффективны при антигельминтном иммунитете). Процесс фагоцитоза усиливают опсонины, обволакивающие объект фагоцитоза. Моноциты составляют 5-10 %, а нейтрофилы 60-70 % лейкоцитов крови. Поступая в ткань моноциты формируют популяцию тканевых макрофагов: купферовские клетки (или звездчатые ретикулоэндотелиоциты печени), микроглия ЦНС, остеокласты костной ткани, альвеолярные и интерстициальные макрофаги).
Процесс фагоцитоза. Фагоциты направленно перемещаются к объекту фагоцитоза, реагируя на хемоаттрактанты: вещества микробов, активированные компоненты комплемемента (С5a, C3a) и цитокины.
Плазмалемма фагоцита обхватывает бактерии или другие корпускулы и собственные поврежденные клетки. Затем объект фагоцитоза окружается плазмалеммой и мембранная везикула (фагосома), погружается в цитоплазму фагоцита. Мембрана фагосомы сливается с лизосомой и фагоцитированный микроб разрушается, pН закисляется до 4,5; активируются ферменты лизосомы. Фагоцитированный микроб разрушается под действием ферментов лизосом, катионных белков дефенсинов, катепсина G, лизоцима и др. факторов. При окислительном (дыхательном) взрыве в фагоците образуются токсичные антимикробные формы кислорода – перекись водорода H2O2, суперосиданион O2-, гидроксильный радикал ОH-, синглетный кислород. Кроме этого антимикробным действием обладают окись азота и радикал NO-.
Макрофаги выполняют защитную функцию еще до взаимодействия с другими иммунокомпетентными клетками (неспецифическая резистентность). Активация макрофага происходит после разрушения фагоцитируемого микроба, его процессинга (переработки) и презентации (представлении) антигена T-лимфоцитам. В заключительную стадию иммунного ответа Т-лимфоциты выделяют цитокины, активирующие макрофаги (приобретенный иммунитет). Активированные макрофаги вместе с антителами и активированным комплементом (С3b) осуществляют более эффективный фагоцитоз (иммунный фагоцитоз), разрушая фагоцитированные микробы.
Фагоцитоз может быть завершенным, завершающимся гибелью захваченного микроба, и незавершенным, при котором микробы не погибают. Примером незавершенного фагоцитоза является фагоцитоз гонококков, туберкулезных палочек и лейшманий.
Все фагоцитирующие клетки организма, по И. И. Мечникову, подразделяются на макрофаги и микрофаги. К микрофагам относятся полиморфно-ядерные гранулоциты крови: нейтрофилы, эозинофилы и базофилы. Макрофаги различных тканей организма (соединительной ткани, печени, легких и др.) вместе с моноцитами крови и их костномозговыми предшественниками (промоноциты и монобласты) объединены в особую систему мононуклеарных фагоцитов (СМФ). СМФ филогенетически более древняя по сравнению с иммунной системой. Она формируется в онтогенезе достаточно рано и имеет определенные возрастные особенности.
Микрофаги и макрофаги имеют общее миелоидное происхождение - от полипотентной стволовой клетки, которая является единым предшественником грануло- и моноцитопоэза. В периферической крови содержится больше гранулоцитов (от 60 до 70 % всех лейкоцитов крови), чем моноцитов (от 1 до 6 %). Вместе с тем длительность циркуляции моноцитов в крови значительно больше (полупериод 22 ч), чем короткоживущих гранулоцитов (полупериод 6,5 ч). В отличие от гранулоцитов крови, являющихся зрелыми клетками, моноциты, покидая кровяное русло, в соответствующем микроокружении созревают в тканевые макрофаги. Внесосудистый пул мононуклеарных фагоцитов в десятки раз превышает их число в крови. Особенно богаты ими печень, селезенка, легкие.
Все фагоцитирующие клетки характеризуются общностью основных функций, сходством структур и метаболических процессов. Наружная плазматическая мембрана всех фагоцитов является активно функционирующей структурой. Она отличается выраженной складчатостью и несет множество специфических рецепторов и антигенных маркеров, которые постоянно обновляются. Фагоциты снабжены высокоразвитым лизосомным аппаратом, в котором содержится богатый арсенал ферментов. Активное участие лизосом в функциях фагоцитов обеспечивается способностью их мембран к слиянию с мембранами фагосом или с наружной мембраной. В последнем случае происходит дегрануляция клеток и сопутствующая секреция лизосомных ферментов во внеклеточное пространство.
Фагоцитам присущи три функции:
1 - защитная, связанная с очисткой организма от инфекционных агентов, продуктов распада тканей и т. д.;
2 - представляющая, заключающаяся в презентации антигенных эпитопов на мембране фагоцита;
3 - секреторная, связанная с секрецией лизосомных ферментов и других биологически активных веществ - монокинов, играющих важную роль в иммуногенезе.
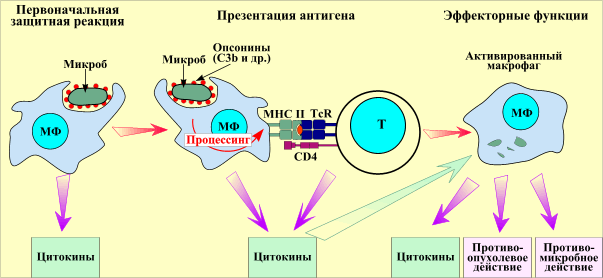
Рис 1. Функции макрофага.
В соответствии с перечисленными функциями различают следующие последовательно протекающие стадии фагоцитоза.
1. Хемотаксис - целенаправленное передвижение фагоцитов в направлении химического градиента хемоаттрактантов в окружающей среде. Способность к хемотаксису связана с наличием на мембране специфических рецепторов для хемоаттрактантов, в качестве которых могут выступать бактериальные компоненты, продукты деградации тканей организма, активированные фракции системы комплемента - С5а, С3а, продукты лимфоцитов- лимфокины.
2. Адгезия (прикрепление) также опосредована соответствующими рецепторами, но может протекать в соответствии с законами неспецифического физико-химического взаимодействия. Адгезия непосредственно предшествует эндоцитозу (захвату).
3. Эндоцитоз является основной физиологической функцией так называемых профессиональных фагоцитов. Различают фагоцитоз - в отношении частиц с диаметром не менее 0,1 мкм и пиноцитоз - в отношении более мелких частиц и молекул. Фагоцитирующие клетки способны захватывать инертные частицы угля, кармина, латекса, обтеканием их псевдоподиями без участия специфических рецепторов. В то же время фагоцитоз многих бактерий, дрожжеподобных грибов рода Саndida и других микроорганизмов опосредован специальными маннозофукозными рецепторами фагоцитов, распознающими углеводные компоненты поверхностных структур микроорганизмов. Наиболее эффективным является фагоцитоз, опосредованный рецепторами, для Fс-фрагмента иммуноглобулинов и для СЗ-фракции комплемента. Такой фагоцитоз называют иммунным, так как он протекает при участии специфических антител и активированной системы комплемента, опсонизирующих микроорганизм. Это делает клетку высокочувствительной к захвату фагоцитами и приводит к последующей внутриклеточной гибели и деградации. В результате эндоцитоза образуется фагоцитарная вакуоль – фагосома. Следует подчеркнуть, что эндоцитоз микроорганизмов в большой степени зависит от их патогенности. Лишь авирулентные или низковирулентные бактерии (бескапсульные штаммы пневмококка, штаммы стрептококка, лишенные гиалуроновой кислоты и М-протеина) фагоцитируются непосредственно. Большинство бактерий, наделенных факторами агрессивности, (стафилококки- А-протеином, кишечные палочки- выраженным капсульным антигеном, сальмонеллы - Vi -антигеном и др.), фагоцитируются, только после их опсонизации комплементом или (и) антителами.
Внутриклеточное переваривание начинается по мере поглощения бактерий или других объектов. Оно происходит в фаголизосомах, образующихся за счет слияния первичных лизосом с фагосомами. Захваченные фагоцитами микроорганизмы погибают в результате осуществления механизмов микробоцидности этих клеток. Различают кислородзависимые механизмы микробоцидности, связанные с окислительным взрывом, и кислороднезависимые механизмы, опосредованные катионными белками и ферментами (в том числе лизоцимом), попадающими в фагосому в результате ее слияния с лизосомами. Так называемый окислительный взрыв проявляется усилением потребления кислорода и глюкозы и одновременным выбросом биологически активных нестабильных продуктов восстановления кислорода: пероксида водорода Н2О2, супероксиданионов О2 , гидроксильных радикалов ОН-. При этом нестабильные кислородные радикалы участвуют в микробоцидности фагоцитов. Внутриклеточная участь захваченных фагоцитами микроорганизмов может быть различной в зависимости от их вирулентности, и способности к внутриклеточному паразитизму. Авирулентные и низковирулентные бактерии погибают и перевариваются в фаголизосомах лизосомными гидролазами.
Незавершенный фагоцитоз заключается в том, что многие вирулентные бактерии часто не погибают и могут длительно персистировать внутри фагоцитов. Факультативно и облигатно внутриклеточные паразиты после эндоцитоза сохраняют жизнеспособность и размножаются внутри фагоцитов, вызывая их гибель и разрушение. Выживание фагоцитированных микроорганизмов могут обеспечивать различные механизмы. Одни патогенные агенты способны препятствовать слиянию лизосом с фагосомами (токсоплазмы, микобактерии туберкулеза) . Другие обладают устойчивостью к действию лизосомных ферментов (гонококки, стафилококки, стрептококки группы А и др.). Третьи после эндоцитоза покидают фагосому, избегая действия микробоцидных факторов, и могут длительно персистировать в цитоплазме фагоцитов (риккетсии и др.). В этих случаях фагоцитоз остается незавершенным.
Презентативная, или представляющая, функция макрофагов состоит в фиксации на наружной мембране антигенных эпитопов микроорганизмов. В таком виде они бывают представлены макрофагами для их специфического распознавания клетками иммунной системы - Т-лимфоцитами.
Секреторная функция заключается в секреции биологически активных веществ - монокинов мононуклеарными фагоцитами. К ним относятся вещества, оказывающие регулирующее действие на пролиферацию, дифференциацию и функции фагоцитов, лимфоцитов, фибробластов и других клеток. Особое место среди них занимает интерлейкин- 1 (ИЛ-1), который секретируется макрофагами. Он активирует многие функции Т-лимфоцитов, в том числе продукцию лимфокина - интерлейкина-2 (ИЛ-2). ИЛ-1 и ИЛ-2 являются клеточными медиаторами, участвующими в регуляции иммуногенеза и разных форм иммунного ответа. Одновременно ИЛ-1 обладает свойствами эндогенного пирогена, поскольку он индуцирует лихорадку, действуя на ядра переднего гипоталамуса. Макрофаги продуцируют и секретируют такие важные регуляторные факторы, как простагландины, лейкотриены, циклические нуклеотиды с широким спектром биологической активности.
Наряду с этим фагоциты синтезируют и секретируют ряд продуктов с преимущественно эффекторной активностью: антибактериальной, антивирусной и цитотоксической. К ним относятся кислородные радикалы (О2, Н2О2), компоненты комплемента, лизоцим и другие лизосомные ферменты, интерферон. За счет этих факторов фагоциты могут убивать бактерии не только в фаголизосомах, но и вне клеток, в ближайшем микроокружении. Этими секреторными продуктами может быть опосредовано также цитотоксическое действие фагоцитов на различные клетки-мишени в клеточно-опосредованных реакциях иммунитета, например в реакции гиперчувствительности замедленного типа (ГЗТ), при отторжении гомотрансплантатов, в противоопухолевом иммунитете.
Рассмотренные функции фагоцитирующих клеток обеспечивают их активное участие в поддержании гомеостаза организма, в процессах воспаления и регенерации,- в неспецифической противоинфекционной защите, а также в иммуногенезе и реакциях специфического клеточного иммунитета (ГЗТ). Раннее вовлечение фагоцитирующих клеток (сначала - гранулоцитов, затем - макрофагов) в ответную реакцию на любую инфекцию или какое-либо повреждение объясняется тем, что микроорганизмы, их компоненты, продукты некроза тканей, белки сыворотки крови, вещества, секретируемые другими клетками, являются хемоаттрактантами для фагоцитов. В очаге воспаления происходит активация функций фагоцитов. Макрофаги приходят на смену микрофагам. В тех случаях, когда воспалительной реакции с участием фагоцитов оказывается недостаточно для очищения организма от возбудителей, тогда секреторные продукты макрофагов обеспечивают вовлечение лимфоцитов и индукцию специфического иммунного ответа.
Естественные клетки киллеры. В организме человека и животных функционирует популяция лимфоцитоподобных клеток, обладающих естественной цитотоксичностью по отношению к клеткам-мишеням. Они получили название естественных клеток- киллеров (ЕКК). ЕКК являются клетками с эффекторной противоопухолевой, противовирусной и противопаразитарной активностью. Они способны спонтанно, без предварительного контакта с антигеном убивать опухолевые клетки, а также клетки, зараженные некоторыми вирусами или паразитами. По-видимому, основной функцией ЕКК является противоопухолевый «надзор». Эта система неспецифической клеточной защиты, вероятно, является филогенетически более древней по сравнению со специфическими Т-клеточными механизмами иммунитета. Морфологически ЕКК представляют собой большие гранулосодержащие лимфоциты. Характерные для них азурофильные цитоплазматические гранулы являются аналогами лизосом фагоцитирующих клеток. Однако ЕКК фагоцитарной функцией не обладают. Неспецифический характер их цитотоксического действия отличает эти клетки от антигенспецифических Т-киллеров и от К-клеток, опосредующих антителозависимую цитотоксичность. Среди лейкоцитов крови человека ЕКК составляют от 2 до12% .
Система комплемента.Системой комплемента называют многокомпонентную самособирающуюся систему белков сыворотки крови, которая играет важную роль в поддержании гомеостаза. Она способна активироваться в процессе самосборки, т. е. последовательного присоединения к образующемуся комплексу отдельных белков, которые называются компонентами, или фракциями комплемента. Таких фракций известно девять. Они продуцируются клетками печени, мононуклеарными фагоцитами и содержатся в сыворотке крови в неактивном состоянии. Процесс активации комплемента может запускаться (инициироваться) двумя разными путями, получившими названия классический и альтернативны.
При активации комплемента классическим путем инициирующим фактором является комплекс антиген - антитело (иммунный комплекс). Причем антитела только двух классов IgG и IgM в составе иммунных комплексов могут инициировать активацию комплемента благодаря наличию в структуре их Fс- фрагментов участков, связывающих С1- фракцию комплемента. При присоединении С1 к комплексу антиген - антитело образуется фермент (С1-эстераза), под действием которого формируется энзиматически активный комплекс (С4b, С2а), называемый С3-конвертазой. Данный фермент расщепляет СЗ на СЗа и СЗb. При взаимодействии субфракции СЗb с С4 и С2 образуется пептидаза, действующая на С5. Если инициирующий иммунный комплекс связан с клеточной мембраной, то самособирающийся комплекс С1, С4, С2, СЗ обеспечивает фиксацию на ней активированной фракции С5, а затем С6 и С7. Последние три компонента совместно способствуют фиксации С8 и С9. При этом два набора фракций комплемента - С5а, С6, С7, С8 и С9 - составляют мембраноатакуюший комплекс, после присоединения которого к клеточной мембране клетка лизируется из-за необратимых повреждений структуры ее мембраны. В том случае, если активация комплемента по классическому пути происходит при участии иммунного комплекса эритроцит - антиэритроцитарный Ig, происходит гемолиз эритроцитов; если иммунный комплекс состоит из бактерии и антибактериального Ig, происходит лизис бактерий, (бактериолизис).
Таким образом, при активации комплемента классическим путем ключевыми компонентами являются С1 и СЗ, продукт расщепления которого С3b активирует терминальные компоненты мембраноатакующего комплекса (С5 - С9).
Существует возможность активации СЗ с образованием СЗb при участии СЗ-конвертазы альтернативного пути, т. е. минуя первые три компонента: С1, С4 и С2. Особенность альтернативного пути активации комплемента состоит в том, что инициация может происходить без участия комплекса антиген-антитело за счет полисахаридов бактериального происхождения - липополисахарида (ЛПС) клеточной стенки грамотрицательных бактерий, поверхностных структур вирусов, иммунных комплексов, включающих IgA и IgE .
Дата добавления: 2015-02-10; просмотров: 912; Мы поможем в написании вашей работы!; Нарушение авторских прав |