
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Комплексных соединений
Отношение комплексов к воде определяется их строением. Нейтральные комплексы молекулярного строения ([Pt(NH3)2Cl4], [Fe(CO)5], [Co2(CO)8]) являются либо жидкостями, либо легкоплавкими кристаллическими веществами в зависимости от размеров молекул (энергии межмолекулярного взаимодействия). Все очень плохо растворимы в воде. Заметно лучше смешиваются с неполярными органическими жидкостями (бензол С6Н6, четыреххлористый углерод СCl4). Большинство других веществ представляют собой ионные кристаллы, в структуре которых регулярно чередуются разноименно заряженные ионы островного строения. Среди таких комплексов имеется немало хорошо растворимых в воде веществ. В процессе растворения молекулы воды сначала вступают в ориентационное взаимодействие с ионами, затем наступает этап донорно-акцепторного связывания (гидратация). Гидратированные ионы покидают кристалл и за счет диффузии равномерно распределяются в объеме раствора (см. химическую теорию растворения твердых веществ в воде):
[Ni(NH3)6]SO4 (тв)  [Ni(NH3)6]2+ (р-р) + SO42–(р-р);
[Ni(NH3)6]2+ (р-р) + SO42–(р-р);
K2[HgJ4] (тв)  2К+(р-р) + [HgJ4]2–(р-р).
2К+(р-р) + [HgJ4]2–(р-р).
Процесс растворения таких соединений совпадает с их диссоциацией. Часто ее называют первичной диссоциацией комплексов.
В то же время в полученных растворах не всегда удается выполнить известные качественные реакции на ионы Ni2+ и Hg2+ (см. стр.7). Это говорит о высокой стабильности внутренней сферы. Однако устойчивость комплексного иона не является абсолютной. Такой вывод можно сделать, если использовать более чувствительные реактивы на ионы‑комплексообразователи. Ионы Ni2+ и Hg2+ имеют 3d8 и 5d10 конфигурации, поэтому могут выступать не только акцепторами электронных пар от лигандов при σ–связывании, но и сами могут предоставлять свои d–электроны для дополнительного π–связывания. Таким образом, эти ионы способны хорошо связываться с атомами (лигандами) σ‑донорами и π–акцепторами, например с ионами CN–, S2–:
ПРNi(CN)2= 3.0∙10-23 ПРNiS = 3.2∙10-19
ПРHg(CN)2= 3.0∙10–35 ПРHgS = 4.0∙10–53.
Поэтому при добавлении раствора Na2S в обоих случаях выпадают черные осадки сульфидов. Эти реакции свидетельствуют о том, что внутренняя сфера комплексов все же частично диссоциирует (вторичная диссоциация). Упрощенно соответствующие уравнения можно записать в виде:
[Ni(NH3)6]2+  Ni2+(aq) + 6 NH3(aq)
Ni2+(aq) + 6 NH3(aq)
[HgJ4]2–  Hg2+(aq) + 4 J–(aq)
Hg2+(aq) + 4 J–(aq)
На самом деле необходимо иметь в виду, что при слабо идущей диссоциации лиганды должны отщепляться последовательно, постадийно:
[Ni(NH3)6]2+  [Ni(NH3)5]2+ + NH3
[Ni(NH3)5]2+ [Ni(NH3)5]2+ + NH3
[Ni(NH3)5]2+  [Ni(NH3)4]2+ + NH3
[Ni(NH3)4]2+ [Ni(NH3)4]2+ + NH3
[Ni(NH3)4]2+  [Ni(NH3)3]2+ + NH3
[Ni(NH3)3]2+ [Ni(NH3)3]2+ + NH3
[Ni(NH3)3]2+  [Ni(NH3)2]2+ + NH3
[Ni(NH3)2]2+ [Ni(NH3)2]2+ + NH3
[Ni(NH3)2]2+  [Ni(NH3)]2+ + NH3
[Ni(NH3)]2+ [Ni(NH3)]2+ + NH3
[Ni(NH3)]2+  Ni2+ + NH3 Ni2+ + NH3
| [HgJ4]2– 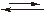 [HgJ3]– + J–
[HgJ3]– [HgJ3]– + J–
[HgJ3]–  [HgJ2] + J–
[HgJ2] [HgJ2] + J–
[HgJ2]  [HgJ]+ + J–
[HgJ]+ [HgJ]+ + J–
[HgJ]+  Hg2+ + J– Hg2+ + J–
|
Константы соответствующих равновесий можно найти в справочной литературе. Их называют частными (ступенчатыми)константами нестойкостикомплексов:
| К1 = 0.93, К2 = 0.19, К3 = 6.5∙10–2, К4 = 1.8∙10–2, К5 = 5.8∙10–3, К6 = 1.7∙10–3 | К1 = 6.0∙10–3, К2 = 1.7∙10–4, К3 = 1.1∙10–11, К4 = 4.5∙10–14 |
Но, строго говоря, эти уравнения также не вполне точны, т.к. в соответствии с ними получается, что КЧ центрального атома постепенно уменьшается и он может в водном растворе полностью "утратить'' свое окружение. На самом же деле в итоге получаются гидратированные ионы, поэтому сам процесс диссоциации следует понимать как последовательную замену соответствующих лигандов на молекулы воды (обсуждать "процесс диссоциации аквокомплексов" в водном растворе вообще бессмысленно):
[Ni(NH3)6]2+ + H2O  [Ni(NH3)5(OH2)]2+ + NH3
[Ni(NH3)5(OH2)]2+ + H2O [Ni(NH3)5(OH2)]2+ + NH3
[Ni(NH3)5(OH2)]2+ + H2O  Ni(NH3)4(OH2)2]2+ + NH3
[Ni(NH3)4(OH2)2]2+ + H2O Ni(NH3)4(OH2)2]2+ + NH3
[Ni(NH3)4(OH2)2]2+ + H2O  [Ni(NH3)3(OH2)3]2+ + NH3
[Ni(NH3)3(OH2)3]2+ + H2O [Ni(NH3)3(OH2)3]2+ + NH3
[Ni(NH3)3(OH2)3]2+ + H2O  [Ni(NH3)2(OH2)4]2+ + NH3
[Ni(NH3)2(OH2)4]2+ + H2O [Ni(NH3)2(OH2)4]2+ + NH3
[Ni(NH3)2(OH2)4]2+ + H2O  [Ni(NH3)(OH2)5]2+ + NH3
[Ni(NH3)(OH2)5]2+ + H2O [Ni(NH3)(OH2)5]2+ + NH3
[Ni(NH3)(OH2)5]2+ + H2O  [Ni(OH2)6]2+ + NH3 [Ni(OH2)6]2+ + NH3
|
[HgJ4]2– + H2O 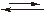 [HgJ3(OH2)]– + J–
[HgJ3(OH2)]– + H2O [HgJ3(OH2)]– + J–
[HgJ3(OH2)]– + H2O  "[HgJ2(OH2)2]" + J–
"[HgJ2(OH2)2]" + H2O "[HgJ2(OH2)2]" + J–
"[HgJ2(OH2)2]" + H2O  [HgJ(OH2)3]+ + J–
[HgJ(OH2)3]+ + H2O [HgJ(OH2)3]+ + J–
[HgJ(OH2)3]+ + H2O  [Hg(OH2)4]2+ + J– [Hg(OH2)4]2+ + J–
|
Однако надо признать, что выглядят эти уравнения довольно громоздко, поэтому записываются в таком виде очень редко. Но именно анализ подобных равновесий позволяет объединить в единую систему разные, на первый взгляд, обменные равновесия в растворах комплексов: замена лигандов, осаждение и растворение осадков, гидролиз, кислотно–основные реакции. Позднее мы немного коснемся этих вопросов.
Вернемся к упрощенным записям уравнений диссоциации внутренней сферы. Промежуточные стадии этих равновесий представляют интерес достаточно редко, но тогда важно понимать, что константа суммарного равновесия представляет собой произведение ступенчатых констант нестойкости:
[Ni(NH3)6]2+  Ni2+ + 6 NH3
Ni2+ + 6 NH3
[HgJ4]2–  Hg2+ + 4 J–
Hg2+ + 4 J–
 = К1·К2·К3·К4·К5·К6 ≈ 2·10–9 (4.1)
= К1·К2·К3·К4·К5·К6 ≈ 2·10–9 (4.1)
 = К1·К2·К3·К4 ≈ 5·10–31 (4.2)
= К1·К2·К3·К4 ≈ 5·10–31 (4.2)
Знание соответствующих констант позволяет прогнозировать возможность (полноту) протекания различных реакций в растворах комплексов. Как известно, равновесия реакций обмена в растворах электролитов смещены в сторону более прочного связывания ионов (в осадки или слабые электролиты, в том числе, в прочные внутренние сферы комплексов). Скажем тот факт, что в растворе тетраиодомеркурата калия трудно получить осадки оксида ртути (II) и иодида свинца легко объяснить на основе анализа следующих равновесий:
K2[HgJ4] + 2 КОН  HgО↓ + Н2О + 4 КJ
HgО↓ + Н2О + 4 КJ
Сокращенное ионное уравнение имеет вид:
[HgJ4]2– + 2ОН–  HgО↓ + Н2О + 4J–
HgО↓ + Н2О + 4J–
Выражение для концентрационной константы данного равновесия выглядит следующим образом:
 . (4.3)
. (4.3)
Если теперь домножить числитель и знаменатель дроби [Hg2+], то получим
 . (4.4)
. (4.4)
Теперь необходимо учесть, что отношение

представляет собой Кн тетраиодомеркурат-иона (см. выражение (4.2)), а произведение [OH–]2·[Hg2+] есть произведение растворимости (ПР) оксида ртути, осадок которого находится в равновесии с гидратированными ионами Hg2+ и ОН–:
HgО↓ + Н2О ⇄ Hg2+ + 2ОН–
Тогда равенство (11.4) может быть представлено в виде
 =
=  ≈ 1.7·10–19. (4.5)
≈ 1.7·10–19. (4.5)
Такое маленькое значение константы равновесия означает, что в стандартных условиях оно протекает с очень низкой полнотой. Это равносильно утверждению, что в составе реагента связывание ионов более прочное, равновесие реакции будет очень сильно смещено влево (в сторону комплекса) и образование осадка очень маловероятно.
Аналогично выглядит ситуация и при попытке осадить иодид свинца. В этом случае можно предположить два варианта реакций и оценить возможности их протекания:
I K2[HgJ4] + 2Pb(NO3)2  2PbJ2↓ + 2KNO3 + Hg(NO3)2
2PbJ2↓ + 2KNO3 + Hg(NO3)2
II K2[HgJ4] + Pb(NO3)2  PbJ2↓ + HgJ2↓ + 2 KNO3
PbJ2↓ + HgJ2↓ + 2 KNO3
В ионном виде:
I HgJ42– + 2Pb2+  2PbJ2↓ + Hg2+
2PbJ2↓ + Hg2+
II HgJ42– + Pb2+  PbJ2↓ + HgJ2↓.
PbJ2↓ + HgJ2↓.
Уже, сравнив ПРиодидов (ПР(PbJ2) = 8∙10–9, ПР(HgJ2) = 4∙10–12), нетрудно понять, что вторая реакция более выгодна: более прочно иодид-ионы связываются с ионами ртути. Проанализируем второе равновесие количественно. Если домножить числитель и знаменатель выражения для концентрационной константы равновесия II на [Hg2+]·[J–]4, то получим
 . (4.6)
. (4.6)
В полученном выражении опять же можно выделить дробь
 ,
,
а, кроме нее, знаменатель равенства (11.6) содержит произведение
[Pb2+]·[J–]2·[Hg2+]·[J–]2,
которое представляет собой произведение растворимости иодидов. Таким образом, получаем для равновесия II
 =
=  ≈ 2.1·10–9. (4.7)
≈ 2.1·10–9. (4.7)
Сравнив значения констант (4.4) и (4.7), можно сделать вывод, что осаждение ионов иода по реакции II более выгодно, чем осаждение оксида HgO, но даже эта реакция характеризуется малой степенью превращения (некоторые шансы появляются только при большом избытке ионов Pb2+в растворе).
Аналогично можно показать, что в растворе сульфата гексаамминникеля (II) сложно получить осадок карбоната никеля (особенно, если учесть, что аммиакаты обычно получают с использованием большого избытка аммиака):
[Ni(NH3)6]SO4 + Na2CO3  NiCO3↓ + 6 NH3 + Na2SO4
NiCO3↓ + 6 NH3 + Na2SO4
или в ионном виде:
[Ni(NH3)6]2+ + CO32–  NiCO3 ↓ + 6 NH3
NiCO3 ↓ + 6 NH3
 =
=  ≈ 1.5·10–2.
≈ 1.5·10–2.
А вот сульфиды никеля (II) и ртути (II) гораздо менее растворимы и осаждаются даже в растворах комплексов. При этом внутренняя сфера центрального атома полностью разрушается:
K2[HgJ4] + Na2S  HgS↓ + 2KNO3 [32]
[HgJ4]2– + S2– HgS↓ + 2KNO3 [32]
[HgJ4]2– + S2–  HgS ↓ + 4J– HgS ↓ + 4J–
 = =  = 1.25·1022 = 1.25·1022
|
[Ni(NH3)6]SO4 + Na2S  NiS ↓ + 6NH3 + Na2SO4
[Ni(NH3)6]2+ + S2– NiS ↓ + 6NH3 + Na2SO4
[Ni(NH3)6]2+ + S2–  NiS ↓ + 6NH3 NiS ↓ + 6NH3
 = =  ≈ 6.25·109 ≈ 6.25·109
|
Оба равновесия сильно смещены вправо, что является результатом прочного связывания ионов Ni2+и Hg2+ с лигандами π-акцепторами.[33]
Итак, эти реакции подтверждают, что внутренняя сфера не является абсолютно устойчивой. Если этот вывод усвоен, то полезно задуматься над вопросом: что представляют собой полученные осадки? Насколько просто устроены вещества с таким простым составом? Насколько данные реакции отличаются от ранее приводившихся примеров реакций замены лигандов?
Оба сульфида являются ионно-ковалентными (для d–металлов характерно такое сочетание типов связей) полимерами с высокими КЧ.
| КЧ: 6 6 NiS Ионы Ni2+ находятся в центрах октаэдров из ионов S2–(КЧ = 6), ионы S2–находятся в центрах треугольных призм из ионов Ni2+ (КЧ = 6). | КЧионов:2+2+…2 HgS Оба типа ионов находятся в центрах сильно искаженных октаэдров: ион Hg2+ связан с шестью партнерами (две связи наиболее прочны, две – очень слабые). Ионы S2–имеют такое же окружение. |
Устроены они бесспорно сложней, чем островные частицы, но по характеру связи соответствуют традиционным комплексам. Принципиальное отличие состоит в том, что ионы S2– выступают в качестве мостиковых лигандов, являются общими для нескольких катионов металлов. Если увеличить концентрацию лигандов в системе, то можно добиться такой ситуации, что их окажется достаточно, чтобы каждый катион Ме2+ смог связаться с собственной группой лигандов и обособиться, отделиться от других. При этом получаться традиционные островные комплексы. Проще деполимеризовать осадок HgS, т.к. каждому иону Ni2+ для этого требуется шесть анионов S2–, а ионы Hg2+ могут "довольствоваться" и четырьмя, а то и двумя лигандами.
HgS ↓ + Na2S р-р  растворение осадка
HgS ↓ + 3Na2S (изб) + 4Н2О растворение осадка
HgS ↓ + 3Na2S (изб) + 4Н2О  Na2[Hg(SH)4] + 4NaOH
HgS ↓ + 3S2–(изб) + 4Н2О Na2[Hg(SH)4] + 4NaOH
HgS ↓ + 3S2–(изб) + 4Н2О  [Hg(SH)4]2– + 4OH–;
Другой вариант описания реакции растворения осадка сульфида ртути может выглядеть следующим образом:
HgS ↓ + S2–(изб) [Hg(SH)4]2– + 4OH–;
Другой вариант описания реакции растворения осадка сульфида ртути может выглядеть следующим образом:
HgS ↓ + S2–(изб)  [HgS2]2– [HgS2]2–
|
NiS ↓ + Na2S р-р  нет признаков реакции
В растворе не удается получить достаточную концентрацию сульфид–ионов. Реакция медленно проходит только с расплавом Na2S. нет признаков реакции
В растворе не удается получить достаточную концентрацию сульфид–ионов. Реакция медленно проходит только с расплавом Na2S.
|
Еще более характерны, разнообразны подобные процессы с участием кислородсодержащих лигандов (ОН2, ОН–, О2–). Замена лигандов в этом случае приводит к процессам гидролиза, полимеризации/деполимеризации, старения осадков гидроксидов. Рассмотрим эти переходы на примере комплексов никеля (+II).
Если светло-желтые кристаллы сульфата никеля растворить в воде, то получим зеленого цвета раствор сульфата гексааквоникеля:
NiSO4 + 6Н2О  [Ni(ОH2)6]SO4 (р-р)
[Ni(ОH2)6]SO4 (р-р)
В этом растворе только молекулы воды способны выступить в качестве лигандов. При этом атом кислорода воды задействует одну из своих неподеленных электронных пар для ковалентного связывания с ионом Ni2+. Мостиковую роль молекулы Н2О выполнять не могут, т.к. это потребует от атома кислорода установления четвертой связи (в аквокомплексе атом кислорода уже образует две связи О–Н и одну связь О–Ni)[34]:
 Более того, за счет поляризующего действия ионов Ni2+ связи О–Н ослабевают, проходит частичный гидролиз аквокомплекса, и среда в растворе становится слабокислой. В упрощенном виде подобные уравнения записывают следующим образом:
Более того, за счет поляризующего действия ионов Ni2+ связи О–Н ослабевают, проходит частичный гидролиз аквокомплекса, и среда в растворе становится слабокислой. В упрощенном виде подобные уравнения записывают следующим образом:
Ni2+ + Н2О  NiOH+ + H+
NiOH+ + H+
NiOH+ + Н2О  "Ni(OH)2"[35] + H+
"Ni(OH)2"[35] + H+
При более строгом рассмотрении реакции гидролиза необходимо уточнить, что речь идет о взаимодействии не "со случайно встреченной молекулой воды", а с собственными лигандами. Причем, конечным продуктом этого процесса может стать полимерный труднорастворимый в воде гидроксид никеля, в составе которого каждый ион Ni2+ связан с шестью группами ОН–, (КЧ(Ni2+) = 6), а каждый ион ОН– связывает трииона Ni2+ (КЧ(ОН–) = 3).18 Поэтому гидролиз аквокомплекса представляет собой сложный полистадийный процесс, сопровождающийся объединением атомов металла за счет мостиковых групп ОН–. Более грамотно первая стадия гидролиза описывается уравнением
[Ni(OH2)6]2+ + [Ni(OH2)6]2+  [(H2O)4Ni(OH)2Ni(OH2)4]2+ + 2H3O+ [36]
[(H2O)4Ni(OH)2Ni(OH2)4]2+ + 2H3O+ [36]
Продуктом реакции является катион тетрааквоникеля (II)-μ-дигидроксо-тетрааквоникеля (II). Упрощая его формулу, часто записывают [Ni(OH)(OH2)4]+ или еще более формально: NiOH+. Уравнения последующих стадий гидролиза объективно составить не представляется возможным, т.к. дальнейшая полимеризация (или точнее, поликонденсация) развивается за счет нескольких параллельно идущих реакций. Надежно можно утверждать только одно: при этом за счет мостиковых гидроксо-групп объединяется все больше никель–кислородных октаэдров.

Чтобы усилить эти процессы, сместить соответствующие равновесия вправо, необходимо нейтрализовывать ионы Н+ (Н3О+), т.е. подщелачивать раствор. Действительно при добавлении раствора NaOH (KOH), наблюдается выпадение осадка гидроксида никеля "Ni(OH)2". Можно сказать, что в этом случае удается полностью заменить в окружении ионов Ni2+ концевые молекулы воды H2O на мостиковые ионы ОН–. Если вместо щелочи добавлять концентрированный раствор аммиака (NH3·H2O), то, казалось бы в систему поставляются новые потенциальные лиганды (NH3) и нужно учесть их возможную конкуренцию с молекулами воды (см. равновесия на стр.280). Но на самом деле первые порции аммиака, попадая в раствор соли никеля, разбавляются, и при этом усиливается диссоциация гидрата:
NH3·H2O (конц)  NH4+ + ОН–;
NH4+ + ОН–;
NH3·H2O (разб)  NH4+ + ОН–
NH4+ + ОН–
Поэтому, наряду с молекулами аммиака, в растворе появляются и гидроксид–ионы с заметной концентрацией. В итоге вместо аммиаката вначале получается осадок Ni(OH)2:
[Ni(OH2)6]2+ + 2 OН–  "Ni(OH)2"↓ + 2 NH4+
"Ni(OH)2"↓ + 2 NH4+
ПР(Ni(OН)2) свежеполученного = 10–15
Хотя, если гидрат аммиака присутствует в системе, в основном, в недиссоциированной форме, более выгодным было бы образование аммиаката:
[Ni(OH2)6]2+ + 2NH3·H2O  "Ni(OH)2"↓ + 2NH4+
"Ni(OH)2"↓ + 2NH4+
 =
=  = 2.25·105.
= 2.25·105.
[Ni(OH2)6]2+ + 6NH3·H2O  [Ni(NH3)6]2+ + 12H2O
[Ni(NH3)6]2+ + 12H2O
 =
=  = 5.0·108.
= 5.0·108.
Полученный осадок гидроксида никеля можно пытаться деполимеризовать, насыщая раствор потенциальными лигандами: аммиаком (NH3·H2O (конц)), гидроксид-ионами (КОН (конц)) или, наоборот, подкисляя раствор и, уменьшая, тем самым, концентрацию лигандов ОН–, вызвавших объединение ионов Ni2+ в полимерный осадок.

В первой реакции в стандартных условиях равновесие достаточно сильно смещено влево. Растворение осадка возможно только в присутствии избытка аммиака.
"Ni(OH)2"↓ + 6 NH3·H2O  [Ni(NH3)6]2++ 2OН– + 6 H2O
[Ni(NH3)6]2++ 2OН– + 6 H2O
 =
=  = 5.0·10–7.
= 5.0·10–7.
Возможность растворения гидроксидов в растворах кислот и щелочей можно продумывать не только с точки стабильности соответствующих аква и гидроксо-комплексов. Спрогнозировать такие реакции можно на основе анализа кислотно-основных свойств гидроксидов. Например, "Ni(OH)2" – это преимущественно основный гидроксид, т.к. поляризующее действие двухзарядного катиона Ni2+ на связь О–Н не очень велика. Поэтому следует ожидать, что в кислотах этот гидроксид будет растворяться гораздо лучше, чем в щелочах, т.е. аквокомплексы для Ni2+ гораздо характерней, чем гидроксо. Не случайно, что нет надежных данных о Кнест комплекса [Ni(OH)6]4–:
Основные свойства: "Ni(OH)2"↓ + 2Н+ + 4H2O  [Ni(OH2)6]2+
[Ni(OH2)6]2+
Нетрудно убедиться,[37] что осадок должен растворяться в кислотах гораздо лучше, чем в избытке раствора аммиака (даже старенный, т.е. частично обезвоженный или длительным хранением, или кипячением раствора с осажденным гидроксидом). Состав старенного Ni(OH)2 принято записывать как NiO·xH2O. Старение осадков гидроксидов приводит к дальнейшей их полимеризации за счет увеличения КЧ аниона по катиону металла. Например, при полном обезвоживании гидроксида никеля получается оксид NiO со структурой NaCl.
| КЧ: 6 3(L: OH–) Ni(OH)2 Кристаллическая форма гидроксида постоянного состава | ||
| 6(L: H2O - 1; OH–- 2 или 3; O2–- 6)[38] NiO·x H2O Гелевая форма свежеполученного осадка гидроксида | 6 (L: OH–- 3; O2–-6) NiO·у H2O "старенный" осадок гидроксида | 6 6 NiO полностью обезвоженный гидроксид |
Кислотные свойства: "Ni(OH)2"↓ + 4 ОН–  [Ni(OH)6]4–
[Ni(OH)6]4–
При нагревании осадка в концентрированных растворах щелочей возможно его незначительное растворение.
 |
Таким образом, следует отметить, что те вещества, которые принято относить к комплексным, генетически связаны с традиционными ионно-ковалентными соединениями. Составляющие особенность островных комплексов реакции ионного обмена зачастую тождественны реакциям осаждения/растворения ионно-ковалентных полимеров (гидроксидов, сульфидов, галогенидов, цианидов…), представляют собой реакции на кислотно-основные свойства осадков. В то же время реакции гидролиза катионов металлов, реакции старения (обезвоживания) осадков их гидроксидов, по сути, тождественны процессу ослабления внутрилигандных связей под влиянием комплексообразователя и могут рассматриваться как реакции замены лигандов в островных (гидролиз) или полимерных (старение) комплексах:
Дата добавления: 2014-11-13; просмотров: 579; Мы поможем в написании вашей работы!; Нарушение авторских прав |