
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Агрегатные состояния вещества. Характер теплового движения в этих состояниях. Особенности теплового движения в различных агрегатных состояниях вещества.
Одним из важнейших параметров, характеризующих молекулу, является минимальная потенциальная энергия взаимодействия 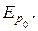 Силы притяжения, действующие между молекулами стремятся сконденсировать вещество, т. е. сблизить его молекулы до расстояния r0, когда их потенциальная энергия взаимодействия минимальна и равна
Силы притяжения, действующие между молекулами стремятся сконденсировать вещество, т. е. сблизить его молекулы до расстояния r0, когда их потенциальная энергия взаимодействия минимальна и равна 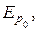 но этому сближению препятствует хаотическое тепловое движение молекул. Интенсивность этого движения определяется средней кинетической энергией молекулы, которая имеет порядок kT, где k – постоянная Больцмана. Агрегатные состояния вещества существенным образом зависят от соотношения величин
но этому сближению препятствует хаотическое тепловое движение молекул. Интенсивность этого движения определяется средней кинетической энергией молекулы, которая имеет порядок kT, где k – постоянная Больцмана. Агрегатные состояния вещества существенным образом зависят от соотношения величин 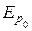 и kT.
и kT.
Предположим, что температура рассматриваемой системы молекул столь высока, что
kT >> 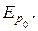 В этом случае интенсивное хаотическое тепловое движение мешает силам притяжения соединить молекулы в агрегаты из нескольких частиц, сблизившихся до расстояния r0: при соударениях большая кинетическая энергия молекул будет легко разбивать эти агрегаты на составляющие молекулы и, таким образом, вероятность образования устойчивых агрегатов будет как угодно малой. В этих обстоятельствах рассматриваемые молекулы, очевидно, будут находиться в газообразном состоянии.
В этом случае интенсивное хаотическое тепловое движение мешает силам притяжения соединить молекулы в агрегаты из нескольких частиц, сблизившихся до расстояния r0: при соударениях большая кинетическая энергия молекул будет легко разбивать эти агрегаты на составляющие молекулы и, таким образом, вероятность образования устойчивых агрегатов будет как угодно малой. В этих обстоятельствах рассматриваемые молекулы, очевидно, будут находиться в газообразном состоянии.
Если температура системы частиц очень низкая, т. е. kT << 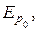 молекулам, действующими силами притяжения, тепловое движение не может помешать приблизиться друг к другу на расстояние близкое к r0в определенном порядке. При этом система частиц будет находиться в твердом состоянии, а небольшая кинетическая энергия теплового движения вынудить молекулы совершать беспорядочные малые колебания около определенных положений равновесия (узлов кристаллической решетки).
молекулам, действующими силами притяжения, тепловое движение не может помешать приблизиться друг к другу на расстояние близкое к r0в определенном порядке. При этом система частиц будет находиться в твердом состоянии, а небольшая кинетическая энергия теплового движения вынудить молекулы совершать беспорядочные малые колебания около определенных положений равновесия (узлов кристаллической решетки).
Наконец, при температуре системы частиц, определяемой из приближенного равенства kT ≈ 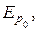 кинетическая энергия теплового движения молекул, величина которой примерно равна потенциальной энергии притяжения, не сможет переместить молекулу на расстояние, существенно превышающее r0. В этих условиях вещество будет находиться в жидком агрегатном состоянии.
кинетическая энергия теплового движения молекул, величина которой примерно равна потенциальной энергии притяжения, не сможет переместить молекулу на расстояние, существенно превышающее r0. В этих условиях вещество будет находиться в жидком агрегатном состоянии.
Таким образом, вещество, в зависимости от своей температуры и величины 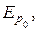 присущей данному сорту составляющих его молекул, будет находиться в газообразном, твердом или жидком состоянии.
присущей данному сорту составляющих его молекул, будет находиться в газообразном, твердом или жидком состоянии.
При нормальных условиях расстояние между молекулами в газе в десятки раз (см. пример 1.1) превышают их размеры; большую часть времени они движутся прямолинейно без взаимодействия и только значительно меньшую часть времени, когда находятся на близких расстояниях от других молекул, взаимодействуют с ними, меняя направление своего движения. Таким образом, в газообразном состоянии движение молекулы выглядит так, как схематично показано на рис.7, а.
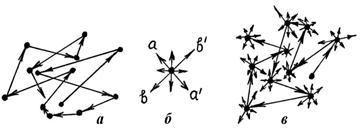
В твердом состоянии каждая молекула (атом) вещества находится в равновесном положении (узел кристаллической решетки), возле которого она совершает малые колебания, причем направление (к примеру, аа' на рис. 7, б) и амплитуда этих колебаний случайно изменяются (к примеру, на направление bb') через время, значительно большее периода этих колебаний; частоты колебаний молекул в общем случае неодинаковы. Колебания отдельной молекулы твердого тела в общих чертах представлена на рис. 7, б.
Молекулы твердого тела упакованы так плотно, что расстояние между ними примерно равно их диаметру, т.е. расстоянию r0 на рис. 3. Известно, что плотность жидкого состояния примерно на 10 % меньше плотности твердого, при прочих равных условиях. Поэтому расстояние между молекулами жидкого состояния несколько больше r0. Учитывая, что в жидком состоянии молекулы обладают еще и большей кинетической энергией теплового движения, следует ожидать, что, в отличие от твердого состояния, они могут, совершая колебательное движение, достаточно легко менять свое местоположение, перемещаясь на расстояние, существенно не превышающее диаметр молекулы. Траектория движения молекулы жидкости приблизительно выглядит так, как схематически показано на рис. 7, в. Таким образом, движение молекулы в жидкости сочетает в себе поступательное движение, как это имеет место в газе, с колебательным, что наблюдается в твердом теле.
Несмотря на неодинаковый характер движения молекул в различных агрегатных состояниях, общим является случайность, непредсказуемость этих движений. Средняя кинетическая энергия этих беспорядочных движений определяет тепловое состояние вещества, его температуру.
Дата добавления: 2015-04-18; просмотров: 525; Мы поможем в написании вашей работы!; Нарушение авторских прав |