
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Вопрос № 10.Восстановление окислов металлов с помощью СО и Н2 .
Восстановление оксидов металлов газами идет по реакциям:


В данном случае  является неизвестным, т.е. неизвестными являются условия восстановления. Анализ можно выполнить, если сопоставить между собой две более простые реакции.
является неизвестным, т.е. неизвестными являются условия восстановления. Анализ можно выполнить, если сопоставить между собой две более простые реакции.




Итак, видим, что  . Чтобы реакция восстановления могла идти вправо, необходимо, чтобы
. Чтобы реакция восстановления могла идти вправо, необходимо, чтобы  было отрицательно. Это может быть достигнуто, если
было отрицательно. Это может быть достигнуто, если  будет более отрицательно, чем величина
будет более отрицательно, чем величина  , значит, у СО (Н2) сродство к кислороду должно быть больше, чем у металла.
, значит, у СО (Н2) сродство к кислороду должно быть больше, чем у металла.
Рассмотрим три крайних случая восстановления оксидов металла газами в зависимости от соотношения между сродством металла к кислороду и сродством восстановителя СО (Н2)к кислороду.
1.Сродство у металла и СО(Н2) к кислороду примерно одинаковы.
Таким образом,  ,
,
Значит 
А т.к. 
Тогда  , а это значит, что в равновесной газовой фазе содержание СО и СО2 примерно одинаково.
, а это значит, что в равновесной газовой фазе содержание СО и СО2 примерно одинаково.
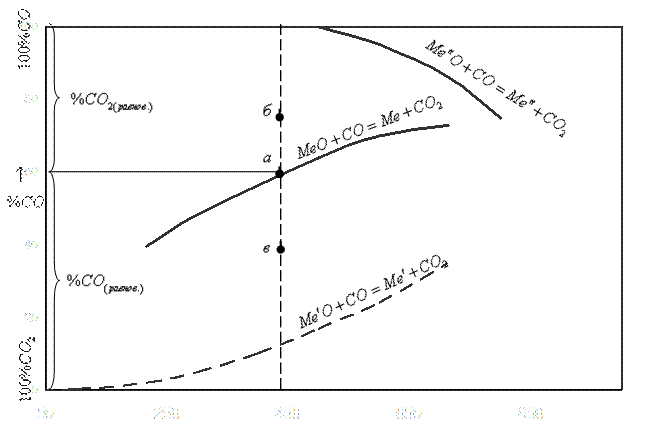
В восстановительной газовой смеси содержание СО должно быть больше, чем в равновесной (см. точку “б”). Если газовая смесь имеет состав в точке “в”, то восстановительный процесс не возможен, а наоборот, может иметь место окисление металла.
Если в газовой фазе содержится только два газа, то  .
.
В этом случае  .
.
В данном случае имеем уравнение с одним неизвестным, из которого находим  .
.
 в том случае, если коэффициенты перед СО и СО2 равны.
в том случае, если коэффициенты перед СО и СО2 равны.
2.Сродство металла к кислороду намного меньше сродства СО к кислороду.
Таким образом, 


 В этом случае
В этом случае  сильно отрицательная величина, следовательно константа равновесия будет большой величиной.
сильно отрицательная величина, следовательно константа равновесия будет большой величиной.



Это значит, что в равновесном газе доля СО2 значительно превышает долю СО.
3.Сродство у металла к кислороду значительно выше, чем у СО.
Таким образом, 


 В этом случае величина
В этом случае величина  будет величиной положительной, а константа равновесия будет очень маленькой величиной.
будет величиной положительной, а константа равновесия будет очень маленькой величиной.



Это значит, что в равновесной газовой фазе доля СО составляет практически 100 %.
Данная схема анализа положена в основу классификации оксидов по восстановимости:
I группа – средневосстановимые оксиды – FeO, SnO, MoO, ZnO.
II группа – легковосстановимые оксиды – NiO, CuO, PbO, MgO.
III группа – трудновосстановимые оксиды – MnO, Al2O3, CaO,V2O3
Газы СО и Н2 имеют практически одинаковые восстановительные свойства, потому что сродство к кислороду у них почти одинаково. Анализ необходимых восстановительных смесей показывает, что газами СО и Н2 рационально восстанавливать средне- и легковосстановимые оксиды металлов, а трудновосстановимые оксиды рациональнее восстанавливать твердым углеродом или металлом – восстановителем.
Дата добавления: 2015-04-21; просмотров: 333; Мы поможем в написании вашей работы!; Нарушение авторских прав |