
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Решение. На каждую степень свободы молекулы газа приходится одинаковая средняя энергия {ε1}= kT, где k – постоянная Больцмана; Т- термодинамическая температура
На каждую степень свободы молекулы газа приходится одинаковая средняя энергия {ε1}=  kT, где k – постоянная Больцмана; Т- термодинамическая температура газа. Так как вращательному движению двухатомной молекулы (молекула кислорода – двухатомная)соответствуют две степени свободы, то средняя энергия вращательного движения молекулы кислорода:
kT, где k – постоянная Больцмана; Т- термодинамическая температура газа. Так как вращательному движению двухатомной молекулы (молекула кислорода – двухатомная)соответствуют две степени свободы, то средняя энергия вращательного движения молекулы кислорода:
{εВр} = 2*  kT. (1)
kT. (1)
Кинетическая энергия вращательного движения всех молекул газа:
Ек = {εВр}N. (2)
Число всех молекул газа:
N = NАv, (3)
где NА – постоянная Авогадро; v – количество вещества.
Если учесть, что количество вещества v = m/M, где m – масса газа; М – молярная масса газа, то формула (3) примет вид: N = NА 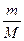 .
.
Подставив выражение N в формулу (2), получим:
Ек = NАm{εВр}/М (4)
Произведем вычисления, учитывая, что для кислорода М = 32*10-3кг/моль (см. табл.14 приложения): {εВр} = kT = 1,38*10-23*350Дж = 4,83*10-21Дж;
Ек = 6,02*1023*  *4,83*10-21Дж = 364Дж.
*4,83*10-21Дж = 364Дж.
Дата добавления: 2015-02-10; просмотров: 289; Мы поможем в написании вашей работы!; Нарушение авторских прав |